Cet épisode de « Du côté du laboratoire » nous conduit, une fois n’est pas coutume, au laboratoire d’immunologie pour s’intéresser à des tests qui explorent l’immunité cellulaire spécifique par le biais de la production d’interférons gamma (IFN-γ). Ces tests sont souvent appelés « IGRA », un acronyme anglais pour interferon gamma release assay car, in fine, ils mesurent la production de cette cytokine par des lymphocytes T placés en présence d’antigènes pour lesquels on souhaite mettre en évidence une immunité cellulaire spécifique préexistante dite « mémoire ». Après quelques rappels sur le principe de ces tests, nous aborderons leur place dans le diagnostic de la tuberculose, un domaine qui a connu des développements importants en remplacement de l’intradermoréaction à la tuberculine, avant d’envisager d’autres applications, notamment dans le champ de la virologie.
Principe des tests d’immunité cellulaire par mesure de la production d’interféron gamma (IGRA)
Rappels sur les interférons
Les interférons (IFN) sont une famille de protéines dotées de propriétés antivirales et immuno-régulatrices qui appartiennent aux protéines dites de signalisation. Ils ne sont pas produits à l’état basal mais leur synthèse est induite par un processus infectieux ou immuno-pathologique [1] (Encadré). L’IFN-γ ou IFNG, encore appelé IFN immunitaire, est le seul représentant des interférons de type II dont la caractéristique est d’être produit principalement par des leucocytes, soit dans le cadre de l’immunité innée sous l’effet d’une activation par la phyto-hémagglutinine A ou, pour les cellules « natural killer1 » (NK), par un processus tumoral, soit dans le cadre de l’immunité adaptative par certains lymphocytes T à la suite d’une stimulation antigénique spécifique, ce qui en fait une lymphokine. Sous l’angle biochimique, l’IFN-γ se présente comme un dimère de deux molécules emboîtées de façon antiparallèle et comportant chacune six hélices alpha. Les réponses cellulaires à l’IFN-γ sont activées par son interaction avec un récepteur hétérodimérique composé des récepteurs d’IFN-γ numéros 1 (IFNGR1) et 2 (IFNGR2). La liaison de l’IFN-γ avec le récepteur active la voie JAK-STAT2 qui contrôle en partie la réponse inflammatoire, l’expression des molécules du complexe majeur d’histocompatibilité de type 1 (CMH1) et la carcinogénèse. Dans l’espèce humaine, le gène de l’IFN-γ (IFNG) est situé sur le chromosome 12.

Bases théoriques des tests d’immunité cellulaire par mesure de la production d’interféron gamma (IGRA)
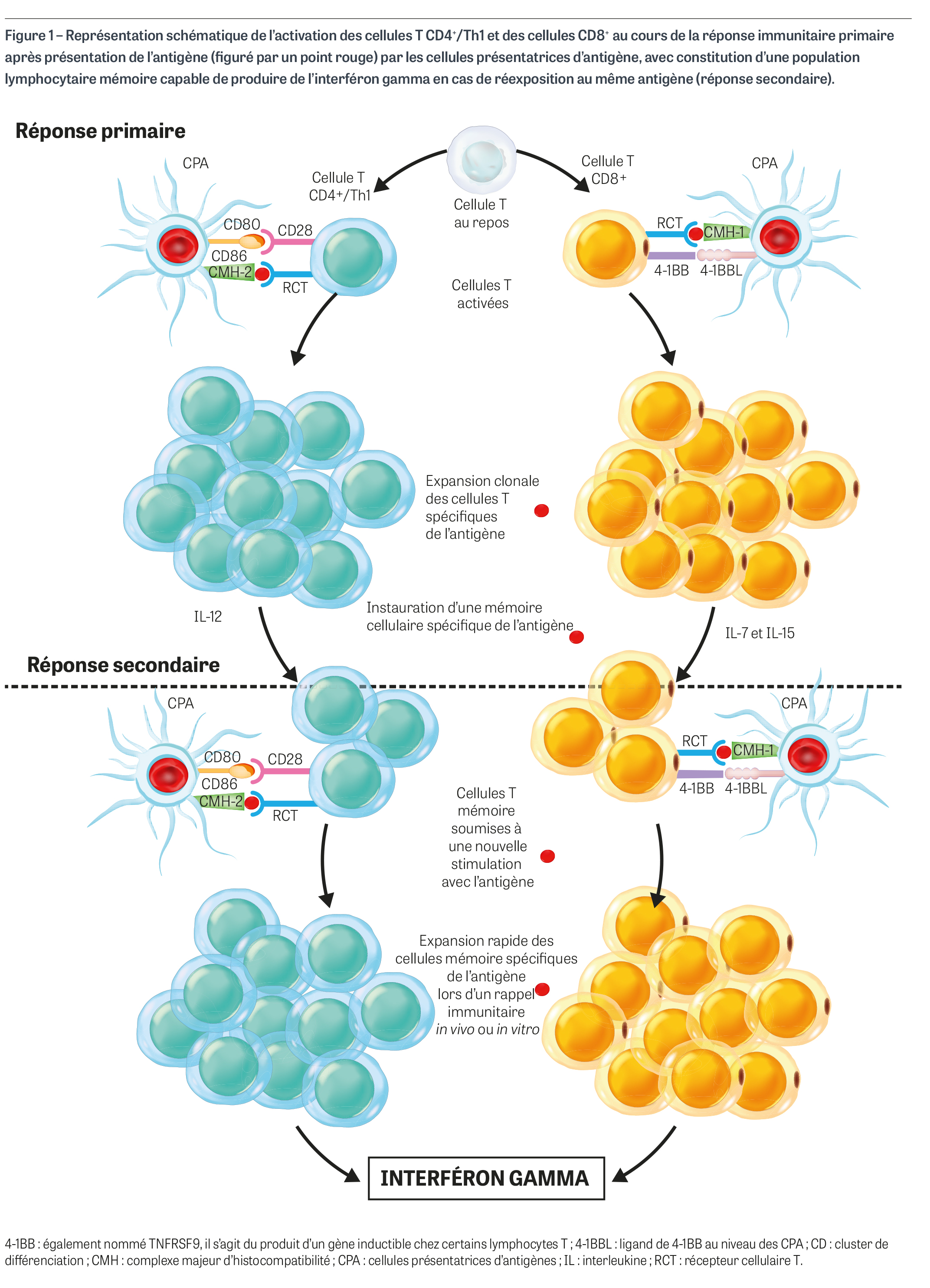
Les tests IGRA sont utilisés pour explorer l’immunité cellulaire mémoire vis-à-vis d’un antigène donné, le plus souvent un agent infectieux. En cas de résultat positif, on peut conclure à une immunité cellulaire préexistante vis-à-vis de l’antigène test ; en cas de résultat négatif, on peut conclure à une absence d’exposition préalable à cet antigène. En pratique, cette mémoire immunitaire est évaluée par la capacité des lymphocytes T exposés à l’antigène à produire de l’IFN-γ considéré comme une lymphokine. Deux types de cellules T sont capables de synthétiser de l’IFN-γ : les lymphocytes CD4+3 orientés dans le sens Th1 et les lymphocytes CD8+ (Figure 1). Les antigènes, capturés par les cellules présentatrices d’antigènes (CPA) comme les monocytes/macrophages ou comme les cellules dendritiques, sont offerts à la reconnaissance des cellules T. Pour qu’un lymphocyte T soit activé par suite de cette stimulation antigénique, trois signaux sont nécessaires :
- le premier signal nécessite la présence d’un récepteur cellulaire T (RCT) capable de reconnaître à la fois l’antigène d’intérêt et une molécule du CMH à la surface des CPA, CMH-2 pour les lymphocytes CD4+ et CMH-1 pour les lymphocytes CD8+, sachant que cette double reconnaissance est indispensable pour permettre l’activation ;
- le deuxième signal est constitué par la présence d’un corécepteur à la surface de la CPA : la cellule CD4+ utilise la molécule CD28 reconnaissant la molécule CD80 (B7-1) ou CD86 (B7-2) sur la CPA, tandis que la cellule CD8+ utilise d’autres corécepteurs comme le 4-1BB qui reconnaît le ligand du 4-1BB (4-1BBL) sur la CPA ;
- une fois ces deux premiers signaux reconnus, la cellule T est activée et présente une expansion clonale ; pour que la cellule CD4+ évolue vers une différenciation de type Th1, synonyme de capacité à produire de l’IFN-γ, un troisième signal externe est nécessaire, à savoir l’interleukine (IL) 124.
L’expansion clonale des cellules T qui correspond à la production de millions de cellules activées spécifiques de l’antigène d’intérêt représente l’aboutissement de la réponse primaire. Ensuite des signaux apoptotiques viennent interrompre cette étape avec néanmoins le maintien de cellules mémoire à longue demi-vie qui perpétuent cette réponse primaire. Dans le cas des cellules T CD8+, des cytokines supplémentaires, l’IL-7 et l’IL-15, sont nécessaires pour pérenniser la mémoire immunitaire. En cas de nouveau contact avec l’antigène par le biais d’une CPA (on parle de réponse secondaire), les lymphocytes T mémoire ont la capacité d’être réactivés en quelques heures (au lieu de plusieurs jours pour la réponse primaire), ce qui entraîne une expansion clonale rapide des cellules T spécifiques de l’antigène ; les cellules CD4+ orientées Th1 et les cellules CD8+ vont alors produire de grandes quantités d’IFN-γ. Ce phénomène s’observe in vivo lors d’un nouveau contact avec l’antigène, mais aussi in vitro au niveau d’un échantillon de sang total. C’est cette dernière propriété qui est mise à profit au cours des tests IGRA pour déterminer si l’individu qui a fourni l’échantillon présente une immunité cellulaire vis-à-vis de l’antigène étudié.
Pour prendre l’exemple de la tuberculose qui sera revu en détail au chapitre suivant, l’intradermoréaction tuberculinique (IDRT) ou test de Mantoux est un test très ancien (1908) qui consiste à injecter au niveau du bras par voie intradermique un échantillon de « tuberculine », une mixture d’environ 200 antigènes dérivée d’un filtrat de bacilles tuberculeux ; les CPA présentent ces antigènes aux cellules T ; en cas d’immunité ancienne consécutive à un premier contact avec un agent de la tuberculose, les cellules T mémoire sont réactivées très rapidement et produisent de nombreuses lymphokines, dont l’IFN-γ, qui participent à une réaction dite d’hypersensibilité retardée dont la conséquence visible pour l’expérimentateur est l’apparition d’une inflammation au point d’injection, matérialisée par une induration du fait de l’afflux de cellules immunitaires sous l’effet des lymphokines produites par les cellules T. Le test d’IDRT est donc un moyen relativement simple d’apprécier in vivo l’existence d’une immunité cellulaire mémoire antituberculeuse. Les tests IGRA ont été développés beaucoup plus récemment (années 1990) pour apporter la même information grâce à une analyse in vitro effectuée sur un échantillon de sang. Les antigènes bactériens sont rajoutés dans le tube et sont phagocytés par les CPA qui les présentent aux lymphocytes T : en cas de mémoire immunitaire préexistante, les cellules T mémoire sont activées en quelques heures et se mettent à produire l’IFN-γ. Grâce au dosage de cette cytokine, il est possible de déduire le statut immunitaire du sujet. Nous reviendrons dans la deuxième partie de l’article sur le cas de l’immunité antituberculeuse.
Considérations pratiques
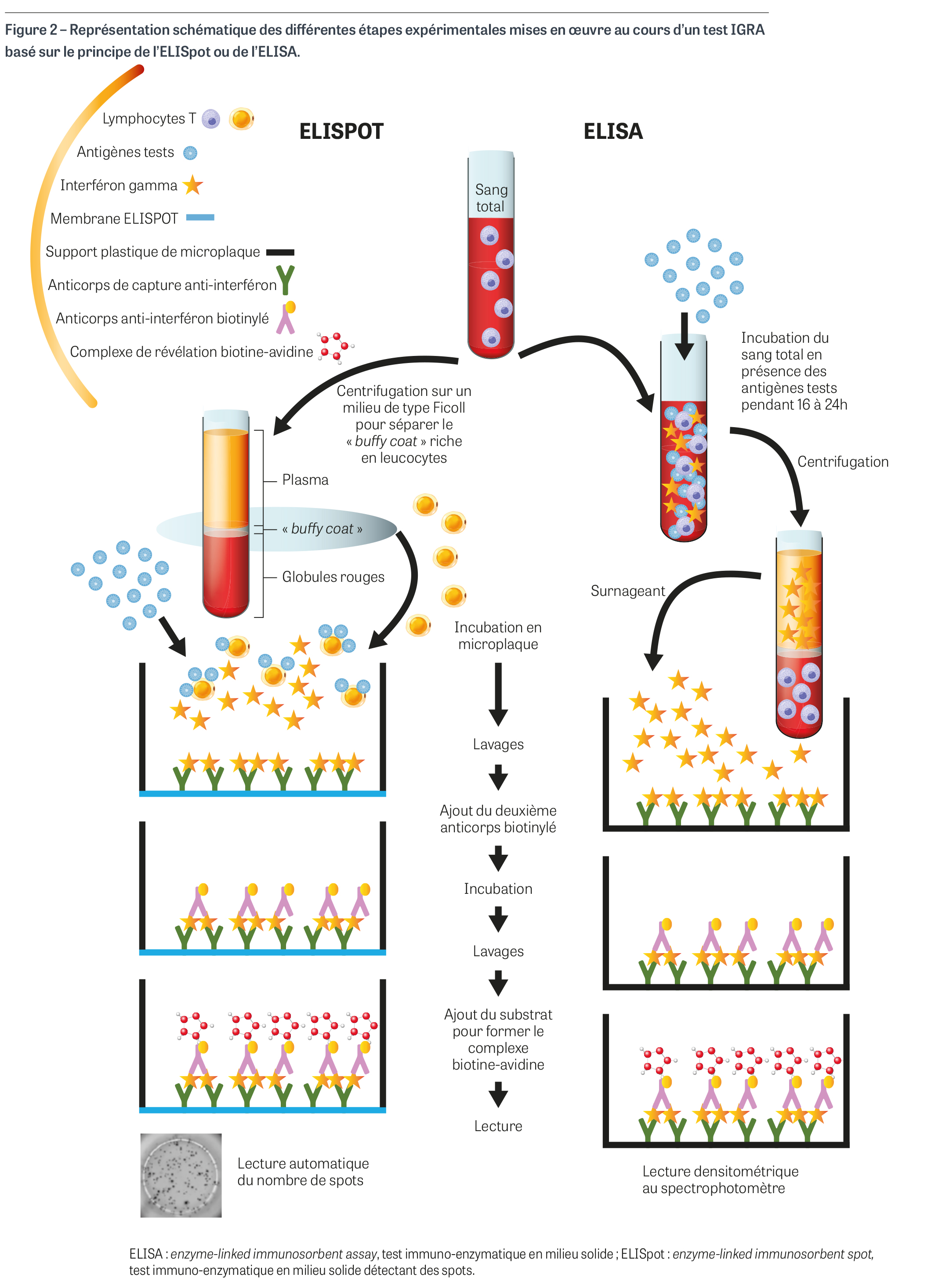
En pratique, on distingue deux types de tests IGRA, tous deux fondés sur la détection de l’IFN-γ dans le cadre d’une réponse mémoire à un ou plusieurs antigènes spécifiques : ceux, les plus nombreux, basés sur une lecture de type ELISA (pour enzyme-linked immunosorbent assay5) ou méthode apparentée (CLIA pour chemiluminescent immunoassay, LFIA pour lateral flow immunoassay ou ELFA pour enzyme-linked fluorescent assay) et ceux basés sur une lecture de type ELISpot6 (enzyme-linked immunosorbent spot) ou FluoroSpot qui détectent directement le nombre de cellules T productrices d’IFN-γ. Ces deux méthodes développées dans les années 1990 sont décrites ci-dessous (Figure 2).
Techniques basées sur le principe ELISA
Les techniques basées sur le principe ELISA utilisent du sang total ; les leucocytes présents dans l’échantillon sont mis en contact avec le ou les antigènes tests pendant 18 à 24 heures ; les CPA captent les antigènes et les présentent aux cellules T spécifiques de ceux-ci ; comme le contact avec les antigènes est bref, seule une réponse mémoire sera détectée sous la forme d’un relargage d’IFN-γ. Il suffit ensuite de centrifuger le tube et de détecter l’IFN-γ présent dans le plasma par un test immuno-enzymatique. La méthode illustrée sur la Figure 2 schématise un test ELISA en microplaque avec un premier anticorps de capture de l’IFN-γ au fond des puits et ajout ultérieur d’un deuxième anticorps anti-IFN-γ marqué à la biotine pour servir de révélateur après addition d’avidine. En général ces tests comportent plusieurs tubes réactionnels : un témoin négatif où l’antigène test ne sera pas incorporé pour vérifier qu’il n’existe pas d’activation non spécifique des cellules T, un témoin positif utilisant un mitogène capable d’activer les lymphocytes T de façon non spécifique, notamment pour s’assurer que la concentration en cellules T est correcte dans l’échantillon, et un ou plusieurs tubes tests pour le ou les antigènes à tester (par exemple des antigènes du bacille tuberculeux dans le cadre de la détection d’une immunité ancienne contre cet agent). La production d’IFN-γ est quantifiée dans chaque puits grâce à une lecture spectrophotométrique du contenu des puits de la microplaque.
Techniques basées sur le principe ELISpot
Les techniques basées sur le principe ELISpot sont dérivées d’un test original décrit en 1983 par Cecil Czerkinsky destiné à visualiser des cellules immunitaires productrices d’anticorps [2] et adapté plus tard à la détection de cellules T productrices de cytokines en réponse à une stimulation antigénique [3]. La technique exige une séparation préalable des leucocytes (buffy coat7) sur un milieu de type Ficoll® (GE Healthcare, Chicago, IL, États-Unis) et leur mise en culture pendant 12 à 48 heures dans une microplaque dont le fond des puits est revêtu d’une membrane de nitrocellulose ou de polyfluorure de vinylidène (PVDF) sur laquelle sont fixés des anticorps anti-IFN-γ. Après addition des antigènes entiers ou des peptides test, les CPA présentent ces derniers aux cellules T mémoire préalablement immunisées ; en réponse à cette activation, les cellules CD4+/Th1 et les cellules CD8+ produisent l’IFN-γ qui est capté par les anticorps fixés au fond de la plaque, aboutissant à la formation d’un spot. Suite à l’addition d’un deuxième anticorps anti-IFN-γ de révélation marqué à la biotine puis à l’addition d’avidine, il apparaît un spot coloré. La plaque est ensuite placée dans un lecteur capable de dénombrer le nombre de spots colorés ou fluorescents qui correspond au nombre de cellules T mémoire productrices d’IFN-γ. Les résultats sont exprimés en cellules T productrices d’IFN-γ (Figure 2). Le contrôle négatif correspond à des puits où les cellules du sujet sont exposées à du milieu de culture dépourvu d’antigène test. Le contrôle positif correspond à des puits où les cellules du sujet sont exposées à un mélange d’anticorps anti-CD3 et anti-CD28 capables d’activer de façon non spécifique les cellules T mémoire.
Application des tests IGRA à la mise en évidence d’une immunité antituberculeuse
La tuberculose : un problème mondial de santé publique
Selon l’Organisation mondiale de la santé (OMS), 10,8 millions (M) d’individus (écart-type compris entre 10,1 M et 11,7 M) étaient atteints de tuberculose active (TBA) dans le monde en 2023, soit une incidence de 134 cas pour 100 000 personnes, et ce chiffre est en constante augmentation (10,1 M en 2020, 10,4 M en 2021 et 10,7 M en 2023). La plupart des cas sont localisés en Asie du Sud-Est (45%), en Afrique (24%) et dans le Pacifique ouest (17%). Parmi eux, 6,1% sont également infectés par le VIH8 [4]. On estime par ailleurs qu’un quart de la population mondiale a été infectée par Mycobacterium tuberculosis (Mtb), le principal agent de la tuberculose (TB). L’histoire naturelle de la tuberculose est importante à connaître pour comprendre sa physiopathologie. Il s’agit d’une infection très répandue transmissible principalement par voie respiratoire par inhalation de particules infectieuses à partir d’individus infectés. Après l’infection, on estime que 80% à 85% des personnes éliminent spontanément la bactérie grâce principalement à leur immunité naturelle. Pour les 20% à 25% de sujets qui conservent la bactérie dans l’organisme, principalement au niveau pulmonaire, le terme d’infection tuberculeuse latente (ITBL ou LTBI en anglais) est utilisé ; cet état d’infection latente est permis grâce à l’instauration d’une immunité spécifique retardée principalement cellulaire. Au sein de la population présentant une ITBL, environ 5% des cas vont présenter dans les deux ans qui suivent la primo-infection une TBA plus ou moins symptomatique et susceptible de participer à la contamination d’autres individus ; une immunodéficience, le jeune âge ou le grand âge, la précarité, les co-infections dont l’infection par le VIH, ainsi que les pathologies tumorales et auto-immunes facilitent cette évolution vers la TBA. Au cours de la vie, les personnes présentant une ITBL peuvent à tout moment réactiver leur infection, notamment si surviennent un ou plusieurs des facteurs de risque énoncés précédemment [5]. Le diagnostic de la TBA est possible grâce à la mise en évidence de Mtb dans les sécrétions respiratoires par des tests bactériologiques (examen direct, culture sur milieux spéciaux, détection du génome bactérien pour les méthodes les plus courantes). Outre les difficultés parfois rencontrées pour affirmer une infection active, notamment quand la charge bactérienne est faible, les deux principales questions qui se posent en pratique clinique sont : comment différencier un individu non immun d’un individu immun vis-à-vis de Mtb, notamment chez les sujets vaccinés par le bacille de Calmette et Guérin (BCG) ? Et comment différencier un individu atteint d’ITBL d’un individu présentant une TBA asymptomatique ou paucisymptomatique ?
Complexité de l’analyse antigénique de M. tuberculosis
Comme cela a été mentionné plus haut, la preuve d’un contact préalable avec un bacille tuberculeux suivi d’une infection latente a longtemps reposé sur la positivité de l’IDRT introduite par Charles Mantoux en 1908. L’antigène utilisé dérive d’une substance provenant de Mtb identifiée par Robert Koch lui-même en 1890 et dénommée « tuberculine » ; c’est la biochimiste américaine Florence Seibert qui a proposé dans les années 1940 ce mélange de quelque 200 protéines purifié à partir de la tuberculine de Koch et appelé PPD (purified protein derivative) de la tuberculine [6]. En plus de la nécessité de revoir le sujet pour lire le résultat du test, de sa traçabilité très relative et du risque de réaction d’hyperréactivité locale, les trois principaux inconvénients de l’IDRT sont : son manque de spécificité du fait de réactions croisées avec des antigènes présents dans des mycobactéries non tuberculeuses et surtout dans le BCG, le seul vaccin (vivant) disponible contre la TB, ce qui ne permet pas de distinguer un sujet infecté naturellement d’un sujet vacciné ; son manque de sensibilité, avec des faux négatifs notamment chez les patients atteints de TBA et dans certaines populations à risque (enfants, infection VIH) ; et sa difficulté technique de réalisation par les personnels de santé, avec notamment la nécessité de réaliser une injection intradermique stricte, ainsi que la subjectivité de la lecture nécessitant des investigateurs entraînés. Des recherches ultérieures ont conduit à l’identification de nouveaux épitopes présents dans le complexe Mycobacterium tuberculosis (comprenant Mtb, M. bovis et M. africanum) qui correspond aux souches responsables de TB chez l’homme, mais absents des souches vaccinales de BCG et des souches de mycobactéries environnementales. Deux épitopes remplissent presque intégralement ce cahier des charges, à savoir ESAT-6 (pour 6 kDa early secreted antigenic target9) et CFP10 (pour 10 kDa culture filtrate protein) : il s’agit de deux peptides de virulence qui forment entre eux un complexe hétérodimérique au sein du complexe M. tuberculosis et qui sont capables d’activer les lymphocytes T mémoire dirigés contre ces bactéries avec une forte production d’IFN-γ ; ils sont absents des souches de BCG. Des réactions croisées peuvent être observées avec seulement trois mycobactéries environnementales, M. kansasii, M. marinum et M. szulgai, la première pouvant être exceptionnellement responsable de tuberculose chez l’humain [7,8]. Ces antigènes ont permis le développement de nouveaux tests d’IDR (Diaskintest® [Generium, Moscou, Russie], EC-skin test [Anhui Zhifei Longcom, Hefei, République populaire de Chine], c-Tb [Statens Serum Institut, Copenhague, Danemark]) avec une spécificité très améliorée par rapport à l’IDR à la tuberculine, notamment chez les sujets vaccinés par le BCG.
Tests IGRA utilisés dans le diagnostic de l’infection tuberculeuse latente
La mise en évidence des nouveaux antigènes décrits au paragraphe précédent a permis dans les années 1990 la mise au point, la standardisation et la commercialisation de tests de type IGRA destinés à se substituer à l’IDRT pour faire le diagnostic d’ITBL. Depuis 2022, trois tests IGRA sont validés par l’OMS dans cette indication [9] :
- un premier test basé sur le principe de l’ELISpot dénommé T-Spot®.TB et commercialisé par Oxford Immunotec au Royaume-Uni (Abingdon) utilisant les antigènes ESAT-6 et CPF10 dans deux tubes séparés, et deux tests basés sur le principe de l’ELISA utilisant les mêmes antigènes ;
- le test QuantiFERON®-TB Gold-Plus (QFT®-Plus) qui est la quatrième génération d’une série de tests produits par la société Qiagen (Hilden, Allemagne) ; cette version comporte notamment deux tubes contenant des antigènes peptidiques issus des antigènes ESAT-6 et CFP-10 ; le tube 2 contient des peptides plus spécifiquement axés sur l’activation des cellules CD8+ ;
- le test Wantai TB-IGRA produit par la société Wantai BioPharm (Pékin, République populaire de Chine).
Plusieurs autres tests IGRA commerciaux sont disponibles sur le marché international [8,10]. On peut citer quelques exemples :
- Qiagen a développé un test QuantiFERON® TB Gold Plus (LIAISON® QFT®-Plus) entièrement automatisé sur l’automate LIAISON® de Diasorin (Saluggia, Italie) avec une lecture en chimioluminescence [11] ;
- Qiagen propose également un test rapide, QIAreach® QuantiFERON®-TB, par technique immunochromatographique à partir d’une cartouche au sein de laquelle s’effectue la réaction de révélation en 20 minutes avec une plateforme de lecture simplifiée qui peut être utilisée en biologie délocalisée [12] ;
- bioMérieux (Marcy-l’Étoile, France) a développé un test complètement automatisé sur sa plateforme VIDAS®10 avec une lecture de type ELFA, le tout sur une période de 17 heures ; les antigènes utilisés sont, comme pour les tests précédents, ESAT-6 et CFP-10 [13].
Avantages et limites des tests IGRA
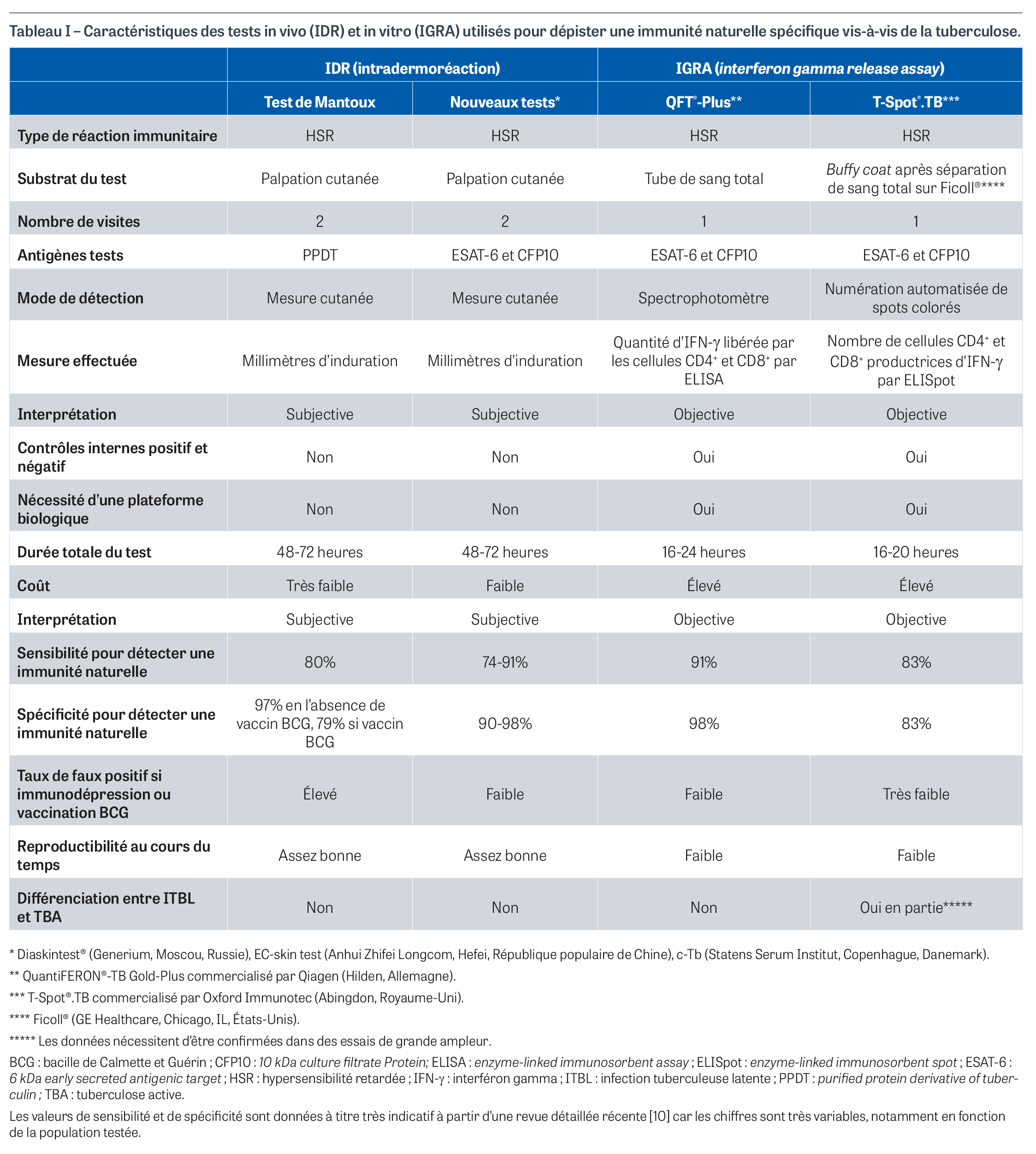
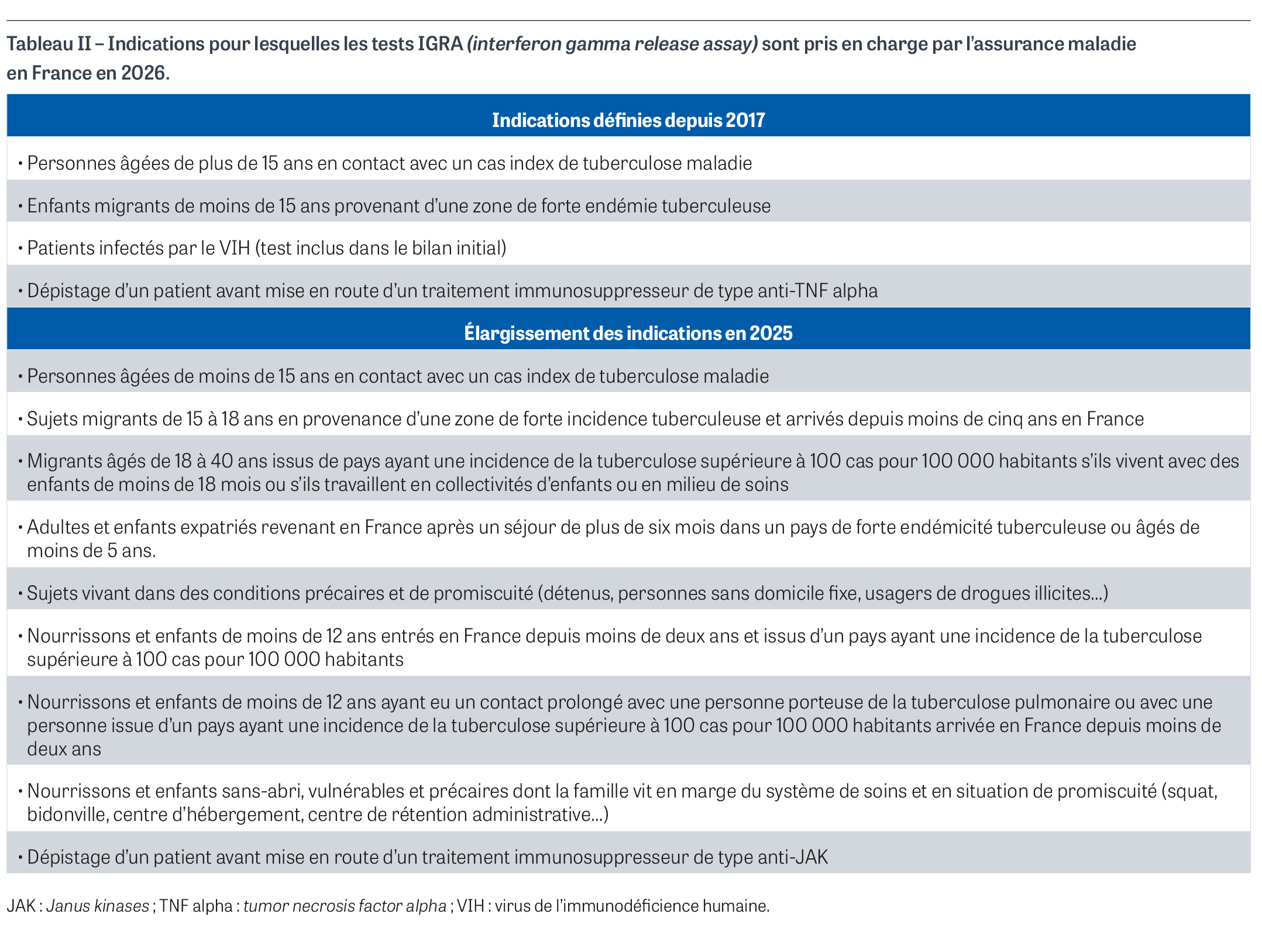
Le tableau I résume les principales caractéristiques, quelques données de performances ainsi que les avantages et inconvénients des tests IGRA en regard de l’lDR [10]. Les valeurs de sensibilité et de spécificité sont données à titre très indicatif à partir d’une revue détaillée récente [10] car les chiffres sont très variables, notamment en fonction de la population testée. Cette difficulté d’évaluer les performances des tests IGRA est directement liée au fait qu’il n’y a pas de test de référence pour évaluer l’immunité cellulaire contre un agent infectieux, ni de valeurs « physiologiques » pour définir un résultat positif ou négatif, ce qui peut conduire à des réponses indéterminées nécessitant de répéter le test. Ce manque de standardisation rend par ailleurs très difficiles les comparaisons entre différents tests. De façon globale, les tests IGRA commerciaux pour la tuberculose se sont solidement implantés dans les pays à ressources économiques élevées et remplacent progressivement les tests cutanés. Cela tient au fait qu’ils sont de mieux en mieux maîtrisés par les laboratoires, notamment du fait de leur standardisation et d’une automatisation de plus en plus complète, et que la pratique de l’IDR demande une grande expérience clinique, avec la nécessité de faire revenir le sujet à distance du geste pour interpréter le résultat. Néanmoins, les deux approches présentent des performances assez similaires, à condition pour l’IDR de remplacer la tuberculine par les antigènes spécifiques (hors BCG) du complexe M. tuberculosis (Tableau I). Dans ses deux avis de 2025, après une analyse très détaillée de la littérature, la Haute Autorité de santé (HAS) conclut que les tests IGRA présentent des performances au moins équivalentes à celles de l’IDR, avec une spécificité diagnostique chez les sujets non vaccinés par le BCG supérieure à 95% et une sensibilité diagnostique comprise entre 80 et 90% [14,15]. Si un résultat positif du test IGRA est faiblement prédictif de l’évolution vers la tuberculose maladie, un test négatif est fortement prédictif d’une absence d’évolution vers cette complication. La HAS émet un avis favorable à un élargissement, par la nomenclature des actes de biologie médicale, des conditions de prise en charge à l’ensemble des sujets présumés immunocompétents à risque de présenter une ITBL (Tableau II). Les tests IGRA sont également utiles pour connaître le statut des soignants vis-à-vis de la tuberculose à l’embauche. La HAS annonce une évaluation dans les mois à venir des données publiées concernant ces tests chez les immunodéprimés. Il existe une littérature très abondante en ce qui concerne la différence d’appréciation des performances des tests IGRA basés sur le principe de l’ELISA ou de l’ELISpot. De façon très schématique, il apparaît que les tests basés sur l’ELISA ou les techniques apparentées (CLIA, LFIA, ELFA) gagnent du terrain en raison de leur plus grande facilité de mise en œuvre en dehors des laboratoires spécialisés en immunologie. En revanche, les tests basés sur l’ELISpot présentent une plus grande sensibilité chez les sujets immunodéprimés en raison de la numération des cellules du buffy coat en amont de la mise en culture, ce qui permet de pallier en partie les numérations faibles de lymphocytes [16,17,18,19]. Par ailleurs, il a été identifié une fluctuation dans le temps des résultats des tests IGRA chez un même sujet, avec de possibles alternances de résultats successifs positifs (conversions) et négatifs (réversions) d’interprétation difficile [20], surtout chez les patients immunodéprimés et pour les valeurs proches du seuil, ce qui fait qu’il est recommandé de ne pas répéter un test positif au cours du temps. Dans les pays à ressources économiques limitées, le développement des tests IGRA se heurte à des difficultés organisationnelles en termes de coût des réactifs et d’infrastructures biologiques capables de réaliser ces tests sur le terrain. Pourtant, un essai récent conduit au Pakistan, une région où l’infection tuberculeuse présente une forte prévalence et où la vaccination par BCG est obligatoire, a montré une plus grande sensibilité des tests IGRA (80% pour le test X.DOT-TB, un test chinois11 basé sur l’ELISpot, et 56% pour le test QFT®-Plus) que celle de l’IDRT (36%) pour identifier une infection tuberculeuse active [21].
Perspectives
Comme rappelé dans le tableau I, les tests IGRA, comme les tests cutanés, sont incapables de différencier de façon indiscutable une ITBL d’une TBA, ce qui pourtant constitue un objectif majeur afin de traiter précocement les sujets contagieux, limiter la dissémination de Mtb et éradiquer la tuberculose, même si les tests basés sur l’ELISpot semblent donner de meilleurs résultats [21]. Pour améliorer ces performances et atteindre pleinement cet objectif, différentes stratégies sont envisagées, notamment identifier des épitopes de Mtb dont l’activation serait significative d’une infection tuberculeuse active [22], ou encore comprendre les déterminismes immunologiques qui protègent les sujets dits « resisters » qui se définissent comme capables de contrôler l’infection sans faire de tuberculose maladie malgré une exposition élevée au risque [23]. Le recours à l’intelligence artificielle est également en cours d’exploration [10].
Utilisation des tests IGRA hors tuberculose
Le succès des tests IGRA dans le domaine de la tuberculose dans les pays à hauts revenus a incité les chercheurs à les appliquer à d’autres pathologies et notamment à certaines infections virales.
Infections à cytomégalovirus humain (HCMV)
Le cytomégalovirus humain (HCMV) est un herpèsvirus qui, une fois la primo-infection survenue, persiste à vie dans l’organisme avec la possibilité de réactivation (et de réinfection avec d’autres souches), notamment au cours de la grossesse et chez les immunodéprimés. Les principales pathologies induites par cet agent s’observent chez le fœtus quand l’infection maternelle a lieu au premier trimestre, et chez les immunodéprimés avec deux populations particulièrement à risque, historiquement les patients atteints de sida et les transplantés d’organes solides et de moelle osseuse allogénique. L’immunité cellulaire joue un rôle capital dans le contrôle des infections à HCMV et, jusqu’à récemment, on manquait d’outils diagnostiques, à côté des tests directs (charge virale ADN12 notamment) et de la sérologie, pour explorer « confortablement » ce versant. La mise à disposition récente au niveau commercial de tests IGRA HCMV a permis de satisfaire en partie ce besoin. Comme pour la tuberculose, deux types de tests sont accessibles, avec trois produits phares : le QuantiFERON®-CMV (QTF-CMV) de la société Qiagen basé sur le principe de l’ELISA, et deux tests basés sur le principe de l’ELISpot, le T-Spot®.CMV de la société Oxford Immunotec (Abingdon, Royaume-Uni) et le T-Track® CMV de la société Mikrogen (Neuried, Allemagne). Les antigènes utilisés pour stimuler les cellules T diffèrent entre les trousses : antigène IE-1 de classe I reconnu exclusivement par les cellules CD8+ pour la première trousse alors que les deux autres trousses utilisent en plus la phosphoprotéine pp65 du CMV qui active à la fois les cellules CD4+ et CD8+. Même si ce sont les cellules CD8+ qui jouent le rôle principal dans la défense contre l’infection à HCMV, cette différence permet d’expliquer des discordances entre les résultats obtenus avec les deux technologies. Sans qu’il soit possible d’entrer dans les détails dans le cadre de cet article de synthèse, les tests IGRA HCMV sont de plus en plus utilisés pour l’exploration des transplantés d’organes solides ou de moelle [24,25,26]. De façon très schématique, ces tests peuvent être utiles pour personnaliser la prise en charge des transplantés, notamment en allégeant les traitements anti-CMV prophylactiques actuellement prescrits à titre systématique, ainsi que la surveillance virologique post-greffe, et en raccourcissant les traitements antiviraux curatifs au décours d’une infection à HCMV post-greffe chez les sujets présentant une bonne réponse immunitaire cellulaire anti-CMV avec les tests IGRA-CMV [27,28,29]. Dans le cadre de l’infection congénitale à HCMV, il existe des arguments pour dire que ces tests pourraient aider à différencier les infections primaires des réactivations, notamment en utilisant les tests ELISpot qui investiguent les réponses CD4+ et CD8+ [30].
Autres infections virales chez l’immunodéprimé
Dans la suite des résultats observés pour HCMV, d’autres réactivations virales peuvent être recherchées chez les immunodéprimés, notamment pour EBV (virus d’Epstein-Barr), HHV-6 (herpèsvirus humain type 6) ou les polyomavirus. Il s’agit le plus souvent de tests IGRA maison [31], même si Qiagen propose au titre de la recherche une trousse QuantiFERON®-EBV ciblant des épitopes de l’antigène EBNA (EBV nuclear antigen) dont les performances sont en cours d’évaluation.
Infections à virus SARS-CoV-2
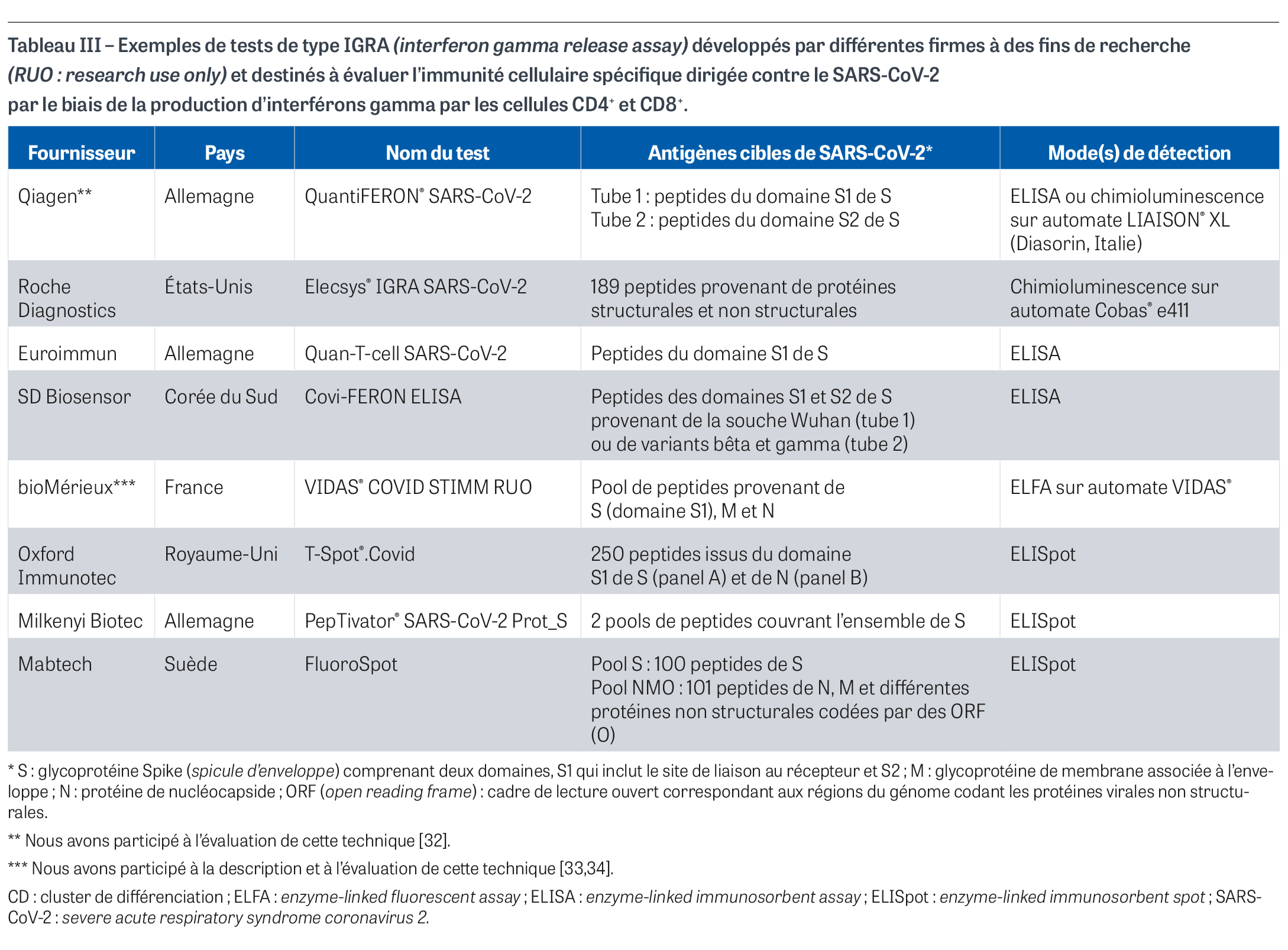
Lors de la pandémie de Covid-1913 qui a émergé fin 2019, il est très vite apparu que l’immunité naturelle puis l’immunité spécifique jouaient un rôle central dans le contrôle de l’infection à SARS-CoV-214 et que son exploration était essentielle à la compréhension de sa physiopathologie. L’arrivée très rapide des tests sérologiques (février 2020) puis de vaccins (décembre 2020) a été suivie un peu plus tard de la nécessité d’explorer la mémoire cellulaire pour essayer de comprendre la labilité de l’immunité anti-SARS-CoV-2 au cours des infections bénignes, de même qu’à la suite de vaccinations successives, avec de grandes disparités entre les individus. Des centaines d’articles ont été publiées depuis 2021 pour essayer de comprendre la place centrale de la mémoire immunitaire cellulaire, et notamment sa spécificité dans la protection à long terme contre cet agent et ses variants successifs. À côté des tests maison développés à cette intention, plusieurs techniques ont été développées avec des firmes commerciales sur le modèle des tests IGRA [32,33,34] (Tableau III). Tous ces tests sont basés sur des pools (groupes) de peptides choisis parmi les antigènes immunodominants du SARS-CoV-2 et sont capables d’activer les cellules CD4+ et CD8+ en déclenchant la sécrétion d’IFN-γ. Ils sont destinés à la recherche et n’ont pas de place dans la prise en charge des patients ni à titre préventif ni à titre curatif. Ils illustrent néanmoins notre capacité à investiguer l’immunité cellulaire de façon beaucoup plus simple et rapide dans le domaine des infections respiratoires virales. Au-delà du Covid-19, il y a fort à parier que cette efflorescence technologique servira de modèle pour d’autres infections virales (grippe, infections à virus respiratoire syncytial…), notamment pour tenter de personnaliser le calendrier des rappels vaccinaux contre ces virus, le rythme annuel préconisé par les autorités sanitaires étant probablement excessif chez un grand nombre de sujets immunocompétents.
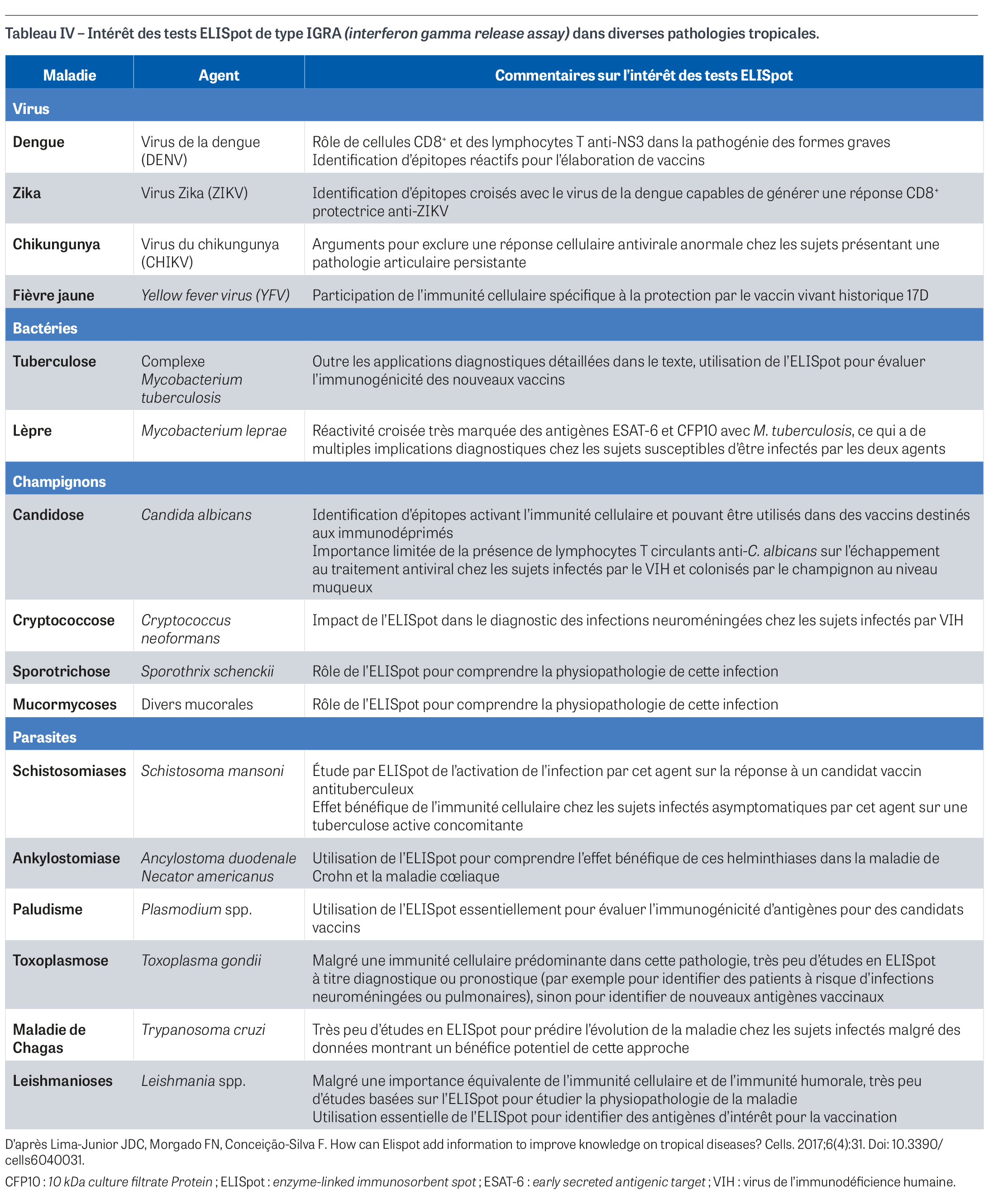
ELISpot et maladies tropicales
Dans le cadre de cette revue, il peut être intéressant d’aborder un dernier thème à la suite de la publication d’un article très original par une équipe brésilienne sur l’intérêt de l’ELISpot dans l’exploration des maladies tropicales, dont la physiopathologie est souvent moins bien comprise que celle des maladies infectieuses couramment observées dans les pays à haut niveau économique [35]. L’exemple de la tuberculose est emblématique de ces pathologies dont l’excès de mortalité touche très majoritairement des régions « tropicales » économiquement défavorisées. Le succès des tests IGRA dans le diagnostic de cette infection pourrait servir de modèle pour d’autres maladies infectieuses dites tropicales. Sans entrer dans le détail de cette revue qui présente un grand nombre de pistes de recherche sur l’exploration immunitaire de différentes pathologies parasitaires, mycosiques, bactériennes et virales par le biais des tests ELISpot dédiés à l’exploration de l’immunité cellulaire spécifique (il convient en effet de rappeler que la première publication de 1983 sur l’ELISpot concernait l’investigation de cellules productrices d’anticorps [2]), le tableau IV liste ces pathologies et quelques publications afférentes basées sur les tests IGRA. Même si la maladie de Lyme n’est pas une pathologie tropicale, ce dernier paragraphe permet aussi de mentionner qu’un test de type IGRA est en développement entre les sociétés Qiagen et Diasorin pour une évaluation combinée de la réponse humorale par sécrétion d’immunoglobulines de classe M ou G (IgM et IgG) et de la réponse spécifique T au cours de l’infection par Borrelia burgdorferi afin de permettre un diagnostic précoce de l’infection, avant la phase sérologique [36]. Ce test, intitulé LIAISON® LymeDetect®, est en cours d’évaluation par la Food and Drug Administration aux États-Unis.
Conclusion
Malgré son rôle prépondérant dans la défense contre les infections, le versant cellulaire de l’immunité spécifique a longtemps souffert d’un déficit de moyens d’exploration fiables, standardisés et relativement simples à mettre en œuvre au lit du patient. Les tests IGRA sont une première réponse à ce besoin et leur succès démontre bien leur utilité. Dans le cadre de la tuberculose et du suivi de certaines infections virales chez l’immunodéprimé, ils sont entrés dans le domaine du soin courant, même si des améliorations techniques et des évaluations plus poussées sont souhaitables pour améliorer leurs performances et leur reproductibilité dans le temps. Pour d’autres pathologies comme les infections respiratoires ou « tropicales », ils sont encore dans la phase exploratoire. De façon globale, l’intérêt de ces investigations réside principalement dans la personnalisation des approches thérapeutiques disponibles, qu’il s’agisse des rappels vaccinaux ou de la mise en place de traitements anti-infectieux préventifs, préemptifs ou curatifs. Par ailleurs, les tests IGRA ne sont qu’un volet très lisible des investigations à venir de l’immunité cellulaire, avec la possibilité de cibler d’autres chimiokines que l’IFN-γ, d’autres cellules que les lymphocytes T ou d’autres pathologies que les maladies infectieuses [37,38], même si la plupart de ces nouveaux tests sont encore du domaine de la recherche clinique. Pour l’hygiéniste, les tests IGRA constituent également un progrès considérable dans la mesure où ils permettent de discriminer les individus en fonction de leur mémoire immunitaire vis-à-vis de pathogènes dont l’arrêt ou le ralentissement de la transmission représente un objectif de santé publique. Dans ce sens, la stratégie « tester et traiter » peut également s’appliquer pour la tuberculose à cette génération de tests.
Notes
1 – Cellules « tueuses naturelles ».
2 – Janus kinases-signal transducer and activator of transcription
proteins, protéines Janus kinases avec transducteur de signal
et activateur de transcription.
3 – CD : cluster de différenciation, « expression désignant
les glycoprotéines membranaires utilisées pour l’identification
et l’immunophénotypage de cellules du système immunitaire »
(Dictionnaire médical de l’Académie de médecine, version 2020).
4 – En parallèle, d’autres chimiokines orientent la cellule CD4+ vers
la différenciation Th2 (IL-4) pour activer la réponse humorale B ou
vers la différenciation Th17 (TGF-ß, IL-6, IL-21, IL-23) qui, par le biais
de l’IL-17A, recrute des neutrophiles contre les infections
bactériennes extracellulaires et fongiques au niveau des
épithéliums et des muqueuses.
5 – Test immuno-enzymatique sur support solide.
6 – Test immuno-enzymatique sur support solide détectant des spots.
7 – Couche leucocytaire.
8 – Virus de l’immunodéficience humaine.
9 – Cible antigénique sécrétée précocement.
10 – VIDAS : VITEK ImmunDiagnostic Assay System, automate
d’immuno-analyse développé par VITEK, filiale américaine
de bioMérieux.
11 – TB Healthcare, Foshan, République populaire de Chine.
12 – Acide désoxyribonucléique.
13 – Coronavirus disease 2019, maladie à coronavirus 2019.
14 – Severe acute respiratory syndrome coronavirus 2, coronavirus 2
du syndrome respiratoire aigu sévère.